Inhalt

Einführung
Die Proteinanalyse ist ein wesentlicher Bestandteil der modernen biologischen und chemischen Forschung. Proteinanalyse bezieht sich auf die Untersuchung von Proteinen, ihren Strukturen, Funktionen und Wechselwirkungen. Diese Untersuchungen sind wichtig, um ein besseres Verständnis von Krankheitsmechanismen, Enzymaktivitäten, zellulären Prozessen und vielem mehr zu erhalten.
Einführung zur Proteinanalyse
Die Proteinanalyse umfasst eine Vielzahl von Techniken, mit denen Proteine identifiziert, charakterisiert und quantifiziert werden können. Diese Techniken reichen von einfachen Methoden wie der Polyacrylamid-Gelelektrophorese (PAGE) bis hin zu fortschrittlicheren Verfahren wie der Massenspektrometrie.
Zu den gängigen Anwendungen der Proteinanalyse gehören die Bestimmung der Proteinmenge, die Identifizierung von spezifischen Proteinen in einer Probe, die Bestimmung von Proteinwechselwirkungen und die Untersuchung von Proteinstrukturen.
Die Proteinanalyse beginnt in der Regel mit der Extraktion der Proteine aus der Probe. Dies kann durch verschiedene Methoden wie Zentrifugation, Lyse oder Immunpräzipitation erfolgen. Anschließend werden die extrahierten Proteine mit verschiedenen Methoden analysiert, um Informationen über ihre Identität und Funktion zu erhalten.
Methoden der Proteinanalyse
Es gibt eine Vielzahl von Methoden, die in der Proteinanalyse verwendet werden. Zu den häufigsten gehören:
- Gelelektrophorese: Eine Methode, bei der Proteine basierend auf ihrer Größe und Ladung in einem Gel separiert werden. Dies ermöglicht die Identifizierung und Quantifizierung von Proteinen.
- Western Blotting: Eine Technik, die verwendet wird, um spezifische Proteine in einer Probe nachzuweisen. Es kann auch verwendet werden, um die Expression von Proteinen zu quantifizieren.
- Massenspektrometrie: Eine fortgeschrittene Methode zur Identifizierung und Quantifizierung von Proteinen. Es ermöglicht die Bestimmung der Molekülmasse und des Peptidmusters eines Proteins.
- Protein-Wechselwirkungsstudien: Methoden wie Co-Immunpräzipitation und Yeast-Two-Hybrid werden verwendet, um die Wechselwirkungen zwischen Proteinen zu untersuchen und ihre Funktionen besser zu verstehen.
- Proteinstrukturanalyse: Methoden wie Röntgenkristallographie und Kernspinresonanzspektroskopie werden verwendet, um detaillierte Informationen über die Struktur von Proteinen zu erhalten.
Diese Methoden und Techniken der Proteinanalyse spielen eine entscheidende Rolle in der biologischen und chemischen Forschung. Sie ermöglichen es Wissenschaftlern, ein besseres Verständnis von Proteinfunktionen und -wechselwirkungen zu erlangen und letztendlich zu neuen Erkenntnissen und Therapien beizutragen.
Beispiel
Ein herausragendes Beispiel für die Proteinanalyse ist die Erforschung von Krebs. Durch die Untersuchung der Proteinexpression und -wechselwirkungen in Krebszellen können Forscher potenzielle Ziele für die Krebstherapie identifizieren. Diese Erkenntnisse können dazu beitragen, neue Medikamente zu entwickeln und die Behandlung von Krebspatienten zu verbessern. Ein erfolgreiches Beispiel für die Anwendung der Proteinanalyse in der Krebsforschung ist die Entdeckung von zielgerichteten Krebstherapien wie dem HER2-Blocker Herceptin.
Die Proteinanalyse spielt eine wichtige Rolle in vielen Bereichen der biologischen und chemischen Forschung. Sie ermöglicht es Wissenschaftlern, die komplexe Welt der Proteine besser zu verstehen und zur Entwicklung neuer Erkenntnisse und Therapien beizutragen.

Proteinextraktion und Präparation
Proteinextraktionstechniken
Die Proteinanalyse beginnt in der Regel mit der Extraktion der Proteine aus einer Probe. Es gibt verschiedene Techniken, die für die Proteinextraktion verwendet werden können. Eine häufig verwendete Methode ist die Zentrifugation, bei der die Proben zentrifugiert werden, um die Proteine zu sedimentieren. Anschließend kann die Proteinfraktion isoliert werden. Eine andere Methode ist die Lyse, bei der die Zellmembranen aufgebrochen werden, um die Proteine freizusetzen. Dies kann durch den Einsatz von Detergenzien oder enzymatischen Verfahren erreicht werden. Eine weitere Methode ist die Immunpräzipitation, bei der Proteine mithilfe von Antikörpern spezifisch aus einer Probe isoliert werden können.
Proteinreinigungsmethoden
Nach der Extraktion der Proteine aus der Probe müssen sie gereinigt werden, um Verunreinigungen zu entfernen und eine bessere Analyse zu ermöglichen. Es gibt verschiedene Methoden zur Proteinreinigung, die je nach den spezifischen Anforderungen angewendet werden können. Eine häufige Methode ist die Affinitätschromatographie, bei der Proteine an eine spezifische Ligandensäule gebunden werden, während andere Komponenten der Probe abgewaschen werden. Nach dem Waschen kann das Protein eluiert und anschließend weiter analysiert werden. Eine andere Methode ist die Ionenaustauschchromatographie, bei der Proteine basierend auf ihrer Ladung separiert werden. Gelchromatographie ist eine weitere Methode, bei der Proteine basierend auf ihrer Größe getrennt werden können.
Die Proteinextraktion und Präparation sind entscheidende Schritte in der Proteinanalyse. Sie ermöglichen es Forschern, die Proteine aus einer Probe zu gewinnen und sie für weitere Untersuchungen vorzubereiten. Durch die Anwendung verschiedener Extraktions- und Reinigungstechniken können hochreine Proteinfraktionen erhalten werden, die für eine detaillierte Analyse geeignet sind.

Proteinquantifizierung und Bestimmung der Reinheit
Spektrophotometrie zur Proteinquantifizierung
Die Proteinquantifizierung ist ein wichtiger Schritt in der Proteinanalyse, um die Konzentration der gewonnenen Proteine zu bestimmen. Eine gängige Methode zur Proteinquantifizierung ist die Spektrophotometrie, bei der die Absorption von Proteinen bei einer bestimmten Wellenlänge gemessen wird. Diese Methode beruht auf dem Lambert-Beer’schen Gesetz, nach dem die Absorption von Licht durch eine Lösung proportional zur Konzentration des gelösten Stoffes ist.
Um die Proteinmenge zu bestimmen, wird eine Absorptionsmessung bei einer spezifischen Wellenlänge durchgeführt. Eine häufig verwendete Wellenlänge für die Proteinquantifizierung ist 280 nm, da die meisten Proteine bei dieser Wellenlänge UV-Licht absorbieren. Durch den Vergleich der gemessenen Absorption mit einer Kalibrierkurve, die mit bekannten Proteinstandards erstellt wurde, kann die Konzentration des Proteins in der Probe berechnet werden.
Elektrophorese zur Bestimmung der Proteinspezifität
Die Elektrophorese ist eine weitere wichtige Methode in der Proteinanalyse, um die Spezifität von Proteinen zu bestimmen. Bei der Elektrophorese werden Proteine basierend auf ihrer Größe und Ladung in einem Gel separiert.
Es gibt verschiedene Arten von Elektrophorese, darunter die native Polyacrylamid-Gelelektrophorese (PAGE) und die denaturierende SDS-PAGE. Bei der native PAGE werden die Proteine in ihrer nativen, dreidimensionalen Struktur analysiert. Die Proteine wandern aufgrund ihrer Größe und Ladung durch das Gel und bilden separate Bänder. Dies ermöglicht die Analyse von Proteinkomplexen und die Bestimmung ihrer Funktionalität.
Bei der denaturierenden SDS-PAGE werden die Proteinproben zuvor mit dem Detergens SDS behandelt, um die Proteine denaturieren und ihre Ladung zu neutralisieren. Dadurch können die Proteine basierend auf ihrer Größe separiert werden. Nach der Elektrophorese können die Proteine mittels einer Färbemethode sichtbar gemacht und analysiert werden.
Diese Elektrophoresemethoden ermöglichen es den Forschern, die Proteinspezifität zu bestimmen und Verunreinigungen zu erkennen. Durch den Vergleich von Proteinmustern in verschiedenen Proben können Änderungen in der Proteinexpression oder Veränderungen in der Proteinstruktur erkannt werden.
Insgesamt sind die Proteinquantifizierung und die Bestimmung der Reinheit wichtige Schritte in der Proteinanalyse. Durch den Einsatz von Spektrophotometrie und Elektrophorese können Forscher die Konzentration der Proteine bestimmen und ihre Spezifität analysieren. Diese Informationen sind entscheidend für weitere Untersuchungen und Experimente in der Proteinforschung.
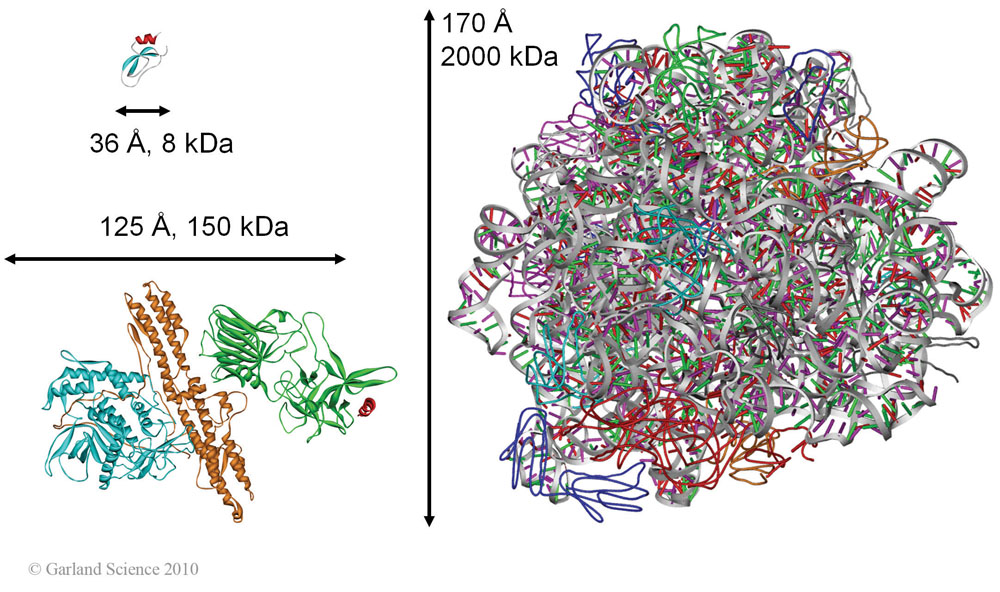
Proteinstrukturanalyse
Proteinstrukturbestimmung mittels Röntgenkristallographie
Die Proteinstrukturbestimmung mittels Röntgenkristallographie ist eine der führenden Methoden in der Proteinanalyse. Sie basiert auf der Nutzung von Röntgenstrahlen, um die dreidimensionale Struktur von Proteinen zu bestimmen. Bei dieser Methode wird das Protein zuerst in kristalliner Form gebracht, indem es in eine Lösung gegeben wird, die dann langsam verdampft. Die entstehenden Proteinmolekülkristalle werden dann mit Röntgenstrahlen bestrahlt.
Die Röntgenstrahlen interagieren mit den Atomen im Protein und erzeugen ein Beugungsmuster. Durch die Analyse dieses Musters können die Positionen der Atome im Protein bestimmt werden. Dies ermöglicht die genaue Darstellung der Proteinstruktur, einschließlich der Lage der Aminosäuren und der räumlichen Anordnung der Proteinbindungstaschen.
Die Proteinstrukturbestimmung mittels Röntgenkristallographie erfordert hochreine Proteinproben und gut kristallisierende Proteine. Zudem ist es eine zeitaufwändige Methode, da das Wachstum von Proteinmolekülkristallen eine gewisse Zeit in Anspruch nimmt. Dennoch liefert sie hochauflösende Strukturinformationen, die für die weitere Forschung von großer Bedeutung sind.
Proteinstrukturanalyse mittels Massenspektrometrie
Die Proteinstrukturanalyse mittels Massenspektrometrie ist eine weitere leistungsstarke Methode in der Proteinanalyse. Sie ermöglicht die Bestimmung der Masse und Struktur von Proteinen. Bei dieser Methode wird das Protein zuerst ionisiert und dann in einem Massenspektrometer analysiert.
Das Massenspektrometer trennt die Ionen basierend auf ihrer Masse-zu-Ladungs-Verhältnis und erzeugt ein Massenspektrum. Durch die Analyse dieses Spektrums können die genaue Masse des Proteins, potenzielle Modifikationen wie Glykosylierungen oder Phosphorylierungen und sogar strukturelle Informationen abgeleitet werden.
Die Proteinstrukturanalyse mittels Massenspektrometrie ist besonders nützlich für die Untersuchung von kleinen bis mittelgroßen Proteinen und deren Interaktionen mit Liganden oder anderen Molekülen. Sie kann auch zur Bestimmung von Protein-Folding und zur Identifizierung von Strukturänderungen bei pathologischen Zuständen eingesetzt werden.
Beide Methoden, Röntgenkristallographie und Massenspektrometrie, sind wichtige Werkzeuge in der Proteinstrukturanalyse. Während die Röntgenkristallographie hochauflösende Strukturinformationen liefert, ermöglicht die Massenspektrometrie eine schnelle und empfindliche Analyse von Proteinproben. Durch den Einsatz dieser Techniken können Forscher ein besseres Verständnis der Proteinstruktur und -funktion erlangen, was wiederum zur Entwicklung neuer therapeutischer Ansätze und Medikamente beitragen kann.

Proteininteraktionen und Funktionen
Protein-Protein-Interaktionsstudien
Proteine interagieren ständig miteinander, um lebenswichtige Funktionen in einer Zelle oder einem Organismus auszuführen. Die Untersuchung dieser Protein-Protein-Interaktionen ist daher von entscheidender Bedeutung, um die zugrunde liegenden Mechanismen biochemischer Prozesse zu verstehen. Es gibt verschiedene Methoden zur Durchführung von Protein-Protein-Interaktionsstudien.
- Co-Immunopräzipitation: Bei dieser Methode werden Antikörper verwendet, um ein bestimmtes Protein aus einer Zelllysate zu immunpräzipitieren. Dadurch können die Wechselwirkungspartner dieses Proteins identifiziert werden.
- Gel Shift Assay: Diese Methode wird verwendet, um die Wechselwirkung zwischen zwei Proteinen nachzuweisen. Dabei wird eine Gel-Elektrophorese durchgeführt und anschließend das Protein analysiert. Änderungen in der Migration des Proteins auf dem Gel können auf eine Protein-Protein-Interaktion hindeuten.
- Hefe-Zwei-Hybrid: Dieses Verfahren nutzt die Signaltransduktion in Hefezellen aus, um Protein-Protein-Interaktionen nachzuweisen. Dabei werden zwei Hybridkonstrukte erzeugt, eines mit dem zu untersuchenden Protein und eines mit einem Aktivierungsdomäne. Wenn die beiden Proteine interagieren, wird die Aktivierungsdomäne aktiviert und ein Reporterprotein wird exprimiert.
Diese Methoden ermöglichen es Forschern, Protein-Protein-Interaktionsnetzwerke zu analysieren und die Rolle von Proteinen in zellulären Signalwegen und biologischen Prozessen zu verstehen.
Funktionsbestimmung von Proteinen
Die Bestimmung der Funktion eines Proteins ist von wesentlicher Bedeutung, um seine Rolle in biologischen Prozessen zu verstehen. Es gibt verschiedene experimentelle Ansätze zur Funktionsbestimmung von Proteinen.
- Genetische Manipulation: Durch das Ausschalten oder Überexprimieren eines bestimmten Gens kann die Funktion des entsprechenden Proteins untersucht werden. Beispielsweise kann ein bestimmtes Gen inaktiviert werden, um die Auswirkungen auf das Organismusverhalten zu beobachten.
- Proteinexpression und Reinigung: Durch die Überexpression und anschließende Reinigung eines Proteins kann seine Funktion in vitro analysiert werden. Verschiedene Assays wie Enzymaktivitätstests oder Bindungsstudien können durchgeführt werden, um die Aktivität und Wechselwirkungen des Proteins zu untersuchen.
- Struktur-Funktions-Analyse: Die Struktur eines Proteins kann Rückschlüsse auf seine Funktion ermöglichen. Durch die Bestimmung der Proteinstruktur können potenzielle Bindungsstellen für Liganden identifiziert werden. Dies kann Hinweise auf die Rolle des Proteins bei spezifischen biologischen Prozessen liefern.
Diese Ansätze zur Funktionsbestimmung von Proteinen sind entscheidend, um das Zusammenspiel von Proteinen in Zellen und Organismen zu verstehen und die Auswirkungen von Mutationen oder Veränderungen im Protein zu untersuchen. Die Kombination verschiedener Methoden ermöglicht es Forschern außerdem, die Funktion unbekannter Proteine zu identifizieren und neue Einblicke in die Biologie zu gewinnen.

Fazit
Die Analyse von Protein-Protein-Interaktionen und die Bestimmung der Funktion von Proteinen sind von entscheidender Bedeutung, um die komplexen Mechanismen in Zellen und Organismen zu verstehen. Protein-Protein-Interaktionen ermöglichen es Forschern, Interaktionsnetzwerke zu erstellen und die Rolle von Proteinen in biologischen Prozessen zu identifizieren. Es gibt verschiedene Methoden zur Durchführung von Protein-Protein-Interaktionsstudien, wie die Co-Immunopräzipitation, den Gel Shift Assay und das Hefe-Zwei-Hybrid-Verfahren.
Die Bestimmung der Funktion eines Proteins kann auf verschiedene Weise erfolgen, wie z.B. durch genetische Manipulation, Proteinexpression und Reinigung sowie Struktur-Funktions-Analyse. Durch diese Ansätze können Forscher die Auswirkungen von Mutationen oder Veränderungen in Proteinen untersuchen und die Interaktionen von Proteinen in Zellen und Organismen besser verstehen.
In Zukunft sind weitere Entwicklungen in der Proteinanalyse zu erwarten. Fortschritte in der Massenspektrometrie und der bioinformatischen Analyse von Proteinsequenzen werden es ermöglichen, Protein-Protein-Interaktionen genauer zu erfassen und Funktionen von Proteinen präziser zu bestimmen. Darüber hinaus könnten neue Technologien und Methoden entwickelt werden, um komplexere Protein-Protein-Interaktionen zu untersuchen und die Funktionen von Proteinen noch besser zu verstehen.
Zusammenfassung und Ausblick auf zukünftige Entwicklungen
Die Analyse von Protein-Protein-Interaktionen und die Bestimmung der Funktion von Proteinen spielen eine wichtige Rolle bei der Erforschung von biologischen Prozessen. Proteine interagieren ständig miteinander, um lebenswichtige Funktionen in Zellen und Organismen auszuführen. Die Untersuchung dieser Interaktionen ermöglicht es Forschern, Interaktionsnetzwerke zu erstellen und die zugrunde liegenden Mechanismen besser zu verstehen.
Es gibt verschiedene Methoden zur Durchführung von Protein-Protein-Interaktionsstudien, wie die Co-Immunopräzipitation, den Gel Shift Assay und das Hefe-Zwei-Hybrid-Verfahren. Diese Methoden ermöglichen es Forschern, Protein-Protein-Interaktionsnetzwerke zu analysieren und die Rolle von Proteinen in zellulären Signalwegen und biologischen Prozessen zu verstehen.
Die Bestimmung der Funktion eines Proteins erfolgt durch genetische Manipulation, Proteinexpression und Reinigung sowie Struktur-Funktions-Analyse. Durch diese Ansätze können Forscher die Auswirkungen von Mutationen oder Veränderungen in Proteinen untersuchen und die Interaktionen von Proteinen in Zellen und Organismen besser verstehen.
Für die Zukunft werden weitere Fortschritte in der Proteinforschung erwartet. Es wird erwartet, dass Fortschritte in der Massenspektrometrie und der bioinformatischen Analyse von Proteinsequenzen die Protein-Protein-Interaktionsstudien verbessern und die Bestimmung der Funktionen von Proteinen präziser machen. Darüber hinaus könnten neue Technologien und Methoden entwickelt werden, um komplexere Protein-Protein-Interaktionen zu untersuchen und die Funktionen von Proteinen noch besser zu verstehen.
Häufig gestellte Fragen
Frage: Warum ist die Analyse von Protein-Protein-Interaktionen wichtig?
Antwort: Die Analyse von Protein-Protein-Interaktionen ist wichtig, um die Rolle von Proteinen in biologischen Prozessen zu verstehen. Proteine interagieren miteinander, um lebenswichtige Funktionen auszuführen, und die Untersuchung dieser Interaktionen ermöglicht es Forschern, die zugrunde liegenden Mechanismen besser zu verstehen.
Frage: Welche Methoden werden zur Durchführung von Protein-Protein-Interaktionsstudien verwendet?
Antwort: Es gibt verschiedene Methoden zur Durchführung von Protein-Protein-Interaktionsstudien, wie die Co-Immunopräzipitation, den Gel Shift Assay und das Hefe-Zwei-Hybrid-Verfahren. Diese Methoden ermöglichen es Forschern, Protein-Protein-Interaktionsnetzwerke zu analysieren und die Rolle von Proteinen in zellulären Signalwegen und biologischen Prozessen zu verstehen.
Frage: Wie können Proteinfunktionen bestimmt werden?
Antwort: Proteinfunktionen können durch genetische Manipulation, Proteinexpression und Reinigung sowie Struktur-Funktions-Analyse bestimmt werden. Diese Ansätze ermöglichen es Forschern, die Auswirkungen von Mutationen oder Veränderungen in Proteinen zu untersuchen und die Interaktionen von Proteinen in Zellen und Organismen besser zu verstehen.












